产品合规
检测/备案/注册
----------写在前面:----------
依据《化妆品监督管理条例》《化妆品生产质量管理规范》《化妆品注册备案管理办法》等相关法规规定,自2021年5月1日起,品牌方想以注册人、备案人的身份开展注册或备案,或是以注册人、备案人的名义在产品标签上体现公司名称和地址,都必须建立质量管理体系

图片截自《化妆品监督管理条例》
新版105条也将于12月1日起正式实施,其中对品牌方质量管理体系提出了具体的要求。品牌方需依据“委托生产版”建立质量管理体系并保证有效运行,以应对即将到来的飞行检查。(再次强调,以上品牌方指作为产品的备案人注册人名义,对于以经销商、授权方等名义体现产品标签上的,不在以下讨论范围)。
本文将依据相关法规要求,结合多年咨询辅导经验,整理并分享化妆品品牌方质量管理体系要求,以及建立和推行方面的注意事项,以供大家参考。
01 检查要点和判定原则介绍
《化妆品生产质量管理规范检查要点和判定原则》委托生产版总共24条,其中重点项目9项(重点项目包括关键项目1项,其他重点项目8项),一般项目15项,关键项目实行1条否决制。具体项目分类和判定原则见下图:
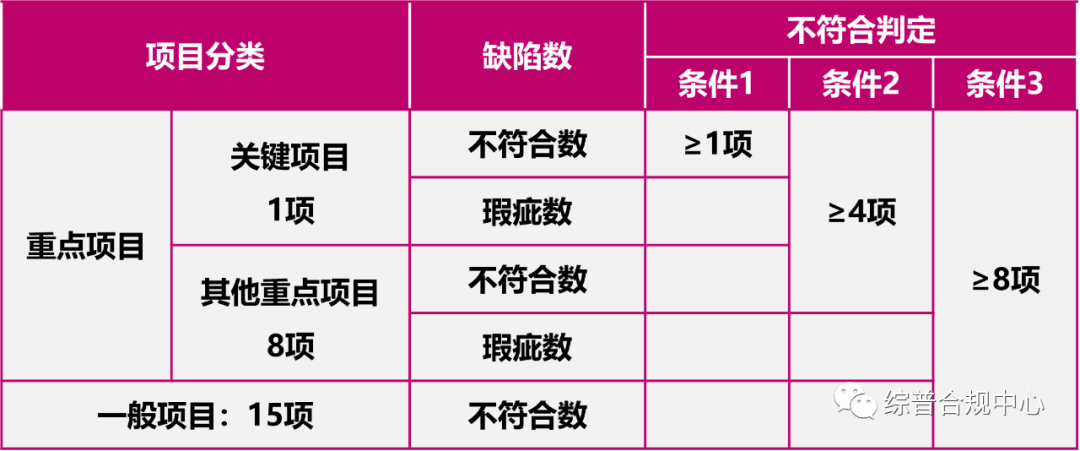
如果现场检查判定为不通过的,会出具“生产质量管理体系存在严重缺陷”的检查结果,同时责令暂停止委托生产和经营,并立案调查 。
如飞行检查中发现不符合第2、4、9、11、12、14、19、20、23、24项的,需立案调查,经调查存在违法行为的,将依法查处。具体涉及违法的条款和关键项目条款内容见下图:
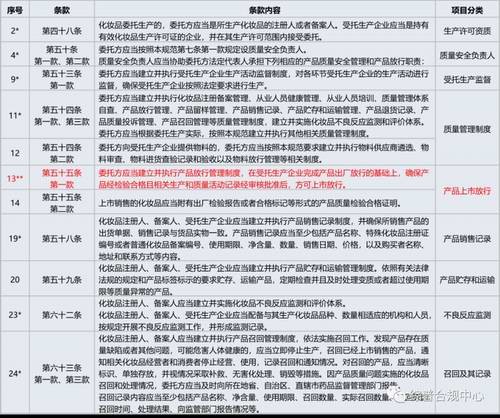
如上所述,品牌方面临的违规风险主要集中在:生产许可资质、质量安全负责人、受托生产监督、质量管理制度、物料管理、产品上市放行、产品销售记录、产品贮存和运输、不良反应监测、产品召回这十个方面。
也就是说,品牌方需优先保证上诉条款符合要求,以避免因行政处罚带来经济损失。下面将依次对上述条款逐一解读合规要求和注意事项。
02 生产许可资质审查
品牌方在委托生产前,必须对受托生产企业的资质进行审核,要求受托生产企业提供营业执照、化妆品生产出许可证。并对受托生产企业资质进行核查,确保受托生产企业《工商营业执照》在有效期内且具有化妆品的生产和经营范围;确保《化妆品生产许可证》在有效期内且载明的生产许可项目符合拟委托的产品类型。

例如:委托产品为气雾灌、散粉类产品,需核查受托方是否具有气雾剂单元、粉单元项目的生产许可。委托生产儿童、眼部化妆品的,需核查生产许可证是否有儿童、和眼部化妆品许可标注。

03 质量安全负责人
质量安全负责人在质量管理中起到承上启下的关键性作用。一个专业的质量安全负责人能结合实际经建立和落实质量管理体系,为企业合法经营、高质量且可持续的发展保驾护航。

1.质量安全负责人资质要求:
品牌方必须设立质量安全负责人岗位,招聘符合要求的专职人员,质量安全负责人需同时符合以下三个条件:
① 专业知识:具备化妆品、化学、化工、生物、医学、药学、食品、公共卫生或者法学等化妆品质量安全相关专业教育或培训背景。可提供符合相关专业学历证明或职业资格证书。
②法规知识:熟悉化妆品相关法律法规、强制性国家标准、技术规范。可提供参加法规相关培训的培训证书。
③ 工作经验:具有5年以上化妆品生产或者质量管理经验。可提供从事化妆品、药品、医疗器械、保健食品、特殊医学用途配方食品、婴幼儿配方食品等行业生产或质量管理工作的工作证明。

2.质量安全负责人工作职责:
品牌方质量安全负责人需履行下列职责,并提供履行相关职责的证据证明。
① 建立并组织实施本企业质量管理体系,落实质量安全管理责任,定期向法定代表人报告质量管理体系运行情况。可提供法人代表签字的内审报告、管理评审报告等。
② 产品质量安全问题的决策及有关文件的签发。可提供质量安全负责人签字的不合格品处理记录、召回决定、报废审批等。
③ 审核化妆品注册、备案资料。可提供经质量安全负责人审核签字的注册、备案资料。
④ 委托方采购、提供物料的,物料供应商、物料放行的审核管理。可提供供应商评审记录及物料放行记录。
⑤ 产品的上市放行。可提供质量安全负责人签字的产品放行记录。
⑥ 受托生产企业遴选和生产活动的监督管理。可提供受托生产企业评审记录和生产活动监督记录或其他证明资料。
⑦ 化妆品不良反应监测管理。可提供不良反应监测、报告、评价记录。
04 受托生产活动监督
品牌方应建立对受托生产企业生产活动的监督制度,规定监督的内容、方式、频次、发现问题的处理方法等。并按照制度规定对受托生产企业生产活动进行监督,确保受托生产企业按照法定要求进行生产,并形成监督记录。

对受托企业的监督方式可以是:定期或随机现场审核、委派驻厂代表、重点物料查验、关键工序在线审批、产品联合检验等方式。相关的监督活动应形成记录并妥善保管,以作为履行生产活动监督职责的证据和免责的依据。

05 质量管理制度
体系文件是质量管理体系的核心内容,品牌方需依据法律法规、国家标准和技术规范的要求,结合企业实际运行情况建立合适的、可操作的质量管理制度。质量管理制度的编制可遵循:写我应做(怎么对就怎么写);做我所写(怎么写就怎么做);记我所做(怎么做就怎么记)的原则,以确保体系文件的适宜性(能不能用),充分性(够不够用),有效性(有没有用)。

依据检查要点及相关法规规定,品牌方质量管理制度至少需涵盖:注册备案、物料采购(如有)、受托生产企业监管、产品放行、贮存、销售、召回、不良反应监测等环节。具体需建立的质量管理制度见下图:

06 产品上市放行
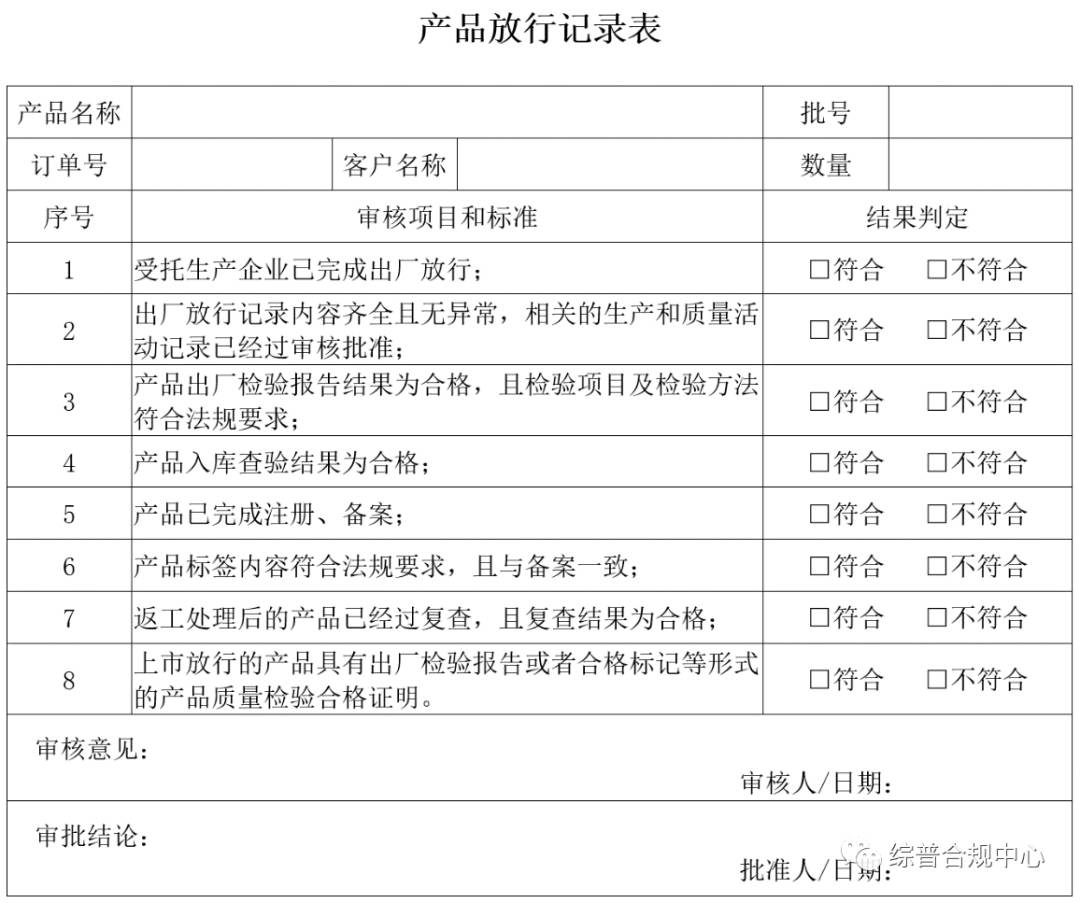
品牌方需在受托生产企业已完成出厂放行的基础上,进行上市前放行审批。放行前需对产品的注册备案凭证、受托生产企业出厂检验报告、受托生产企业出厂放行记录等进行核查,确保产品已完成出厂检验,确保双方生产和质量记录经各自质量安全负责人审核批准后,方可上市销售。

上市销售的化妆品应当附有出厂检验报告或者合格标记等形式的产品质量检验合格证明。质量检验合格证明可以采用:随附的出厂检验报告、内附的“合格证”卡片、印刷或喷码的“合格”标记等形式其中之一来体现。
07 产品销售记录
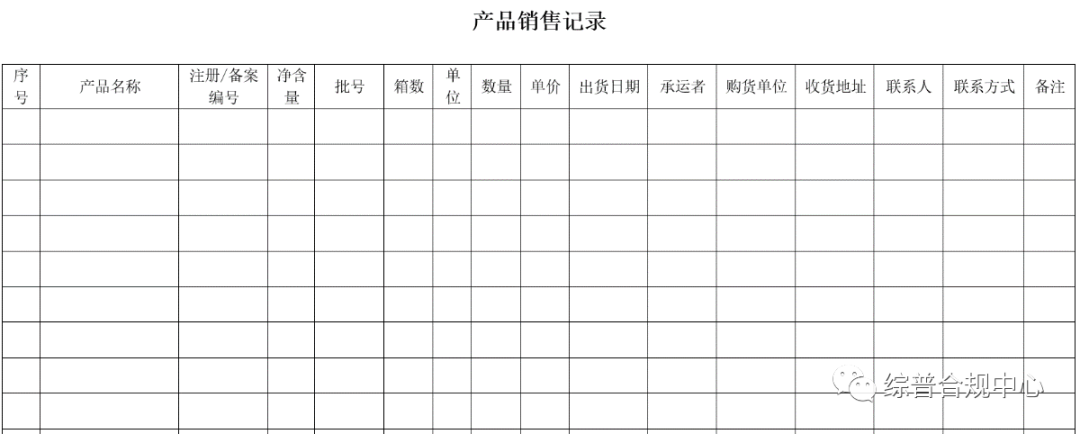
品牌方需建立产品销售记录制度并按照制度规定对所有售出的产品信息及客户信息进行记录,并保证销售记录、出货单据与产品实物信息保持一致。

产品销售记录必须包括产品的名称、批号、注册证号或备案编号、使用期限、净含量、数量、销售日期、价格,以及购买者名称、地址和联系方式等相关信息,以便于问题产品的溯源和召回。销售记录至少保存至产品保质期结束后1年。
08 产品贮存和运输
品牌方需确保产品的贮存、运输环境和卫生条件符合有关法律法规的规定和产品标签标示的要求。对库存产品需定期检查,及时发现并处理变质或者超过使用期限等质量异常的产品。

品牌方需对产品贮存场所的环境温湿度进行监控和记录,并配备必要的虫鼠害防护设施。对运输车辆的防尘、防晒、防水性能,保温、制冷设施和车厢卫生状况等进行检查,并保留检查记录。
品牌方需特别留意产品标签标示的贮存条件。例如:标签标示“阴凉”贮存的,贮存环境和运输车辆温度不得超过20℃,标签标示“避光”保存的,需配制必要的遮阳设施。属于易燃易爆等特种货物的贮存环境和运输车辆需符合相关的法规要求。

09 不良反应监测
品牌方应建立并实施化妆品不良反应监测和评价体系,成立内部不良反应监测机构,指定相关人员负责化妆品不良反应的收集、调查、评价、处理及上报等工作,并形成监测记录。

品牌方应主动收集化妆品不良反应,及时开展评价,调查分析、采取风险控制措施,并向化妆品不良反应监测机构报告。化妆品不良反应遵循“可疑即报”原则,凡是可能与使用化妆品有关的不良反应,均应在《国家化妆品不良反应监测信息系统》进行报告。
10 产品召回
品牌方应建立并执行产品召回管理制度。在发现产品存在质量缺陷或者其他问题,可能危害人体健康时,应当主动召回已经上市销售的产品,通知客户和消费者停止经营和使用,通知受托生产企业停止生产并隔离在制产品。
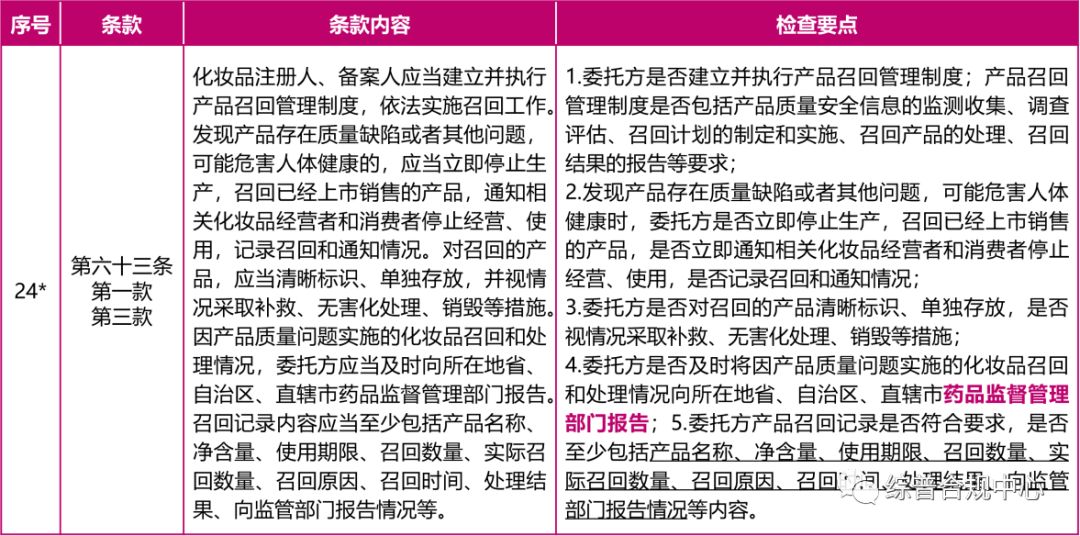
品牌方应建立召回紧急联系人名录,规定召回时的职责和权限。当发现产品存在可能危害人体健康的质量安全问题时,应立即停止生产并实施召回,同时上报至省级药品监督管理部门。
已召回的产品应标注清晰,隔离存放;由质量管理部门进行检验和评估,根据评估结果,确定产品的处理方式,并保留相关记录。
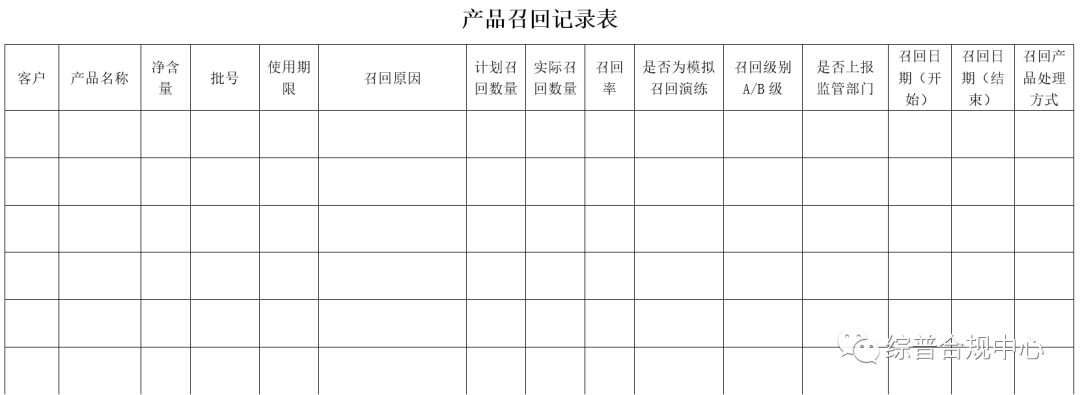
召回记录应包括产品名称、净含量、使用期限、召回数量、实际召回数量、召回原因、召回时间、处理结果、向监管部门报告情况等内容。
小结
新规后,对于品牌方而言,选择成为备案人注册人,就需要重视质量体系的建立和规范,目前有地区已经开始对备案人进行体系的检查或者抽查。
提前执行,有效实施,未雨绸缪,持久合规,才是应对体系监管的有效方式。大家如果在委托方体系落地中遇到以上问题或者需要提供技术支持,可以及时联络综普咨询。