产品合规
备案/注册/咨询/培训
近几年,“外泌体”在护肤与再生医学领域迅速走红。各种“外泌体精华”“外泌体面膜”层出不穷,宣传从保湿修复到抗衰逆龄应有尽有。 但在监管层面,这类产品的身份并不模糊不清——它们可能是化妆品,也可能是药品。
加拿大卫生部(Health Canada)最新发布的通告,就明确了这类产品的分类原则与监管要求。
1. 为什么分类很重要?
在加拿大,《食品与药品法》(Food and Drugs Act, FDA)规定了药品(Drug)、化妆品(Cosmetic)等的定义。 产品的功能、用途、宣传方式,决定了它的监管身份:
分类 | 监管要求 |
药品 | 必须经过临床验证、获批(NOC、DIN)才能上市 |
化妆品 | 需备案(Cosmetic Notification),但不能带有治疗或医疗功能宣传 |
2. 外泌体产品的监管原则
外泌体类物质并非天然就是“药物”,但它们可能因功效、使用方式而被认定为药品。
主要考量因素包括:
1)产品宣称(Representation)
药品:如果宣传“治疗皮肤疾病”“修复细胞”“逆转衰老”等医疗功效,就会被认定为药品。
化妆品:仅限于“改善肤感、保湿、提亮”等美容功效,不涉及治疗。
2)作用水平(Level of Action)
化妆品只作用于表层皮肤,效果应是“轻微且短暂的”;
如果产品需要通过 微针、注射 等方式促进渗透,或必须被吸收发挥系统性作用,那它属于药品。
3)成分组成(Composition)
药品:含有能影响机体功能、具有药理活性的成分。
化妆品:不具备治疗或药理活性。
3. 化妆品 vs 药品:举例对比
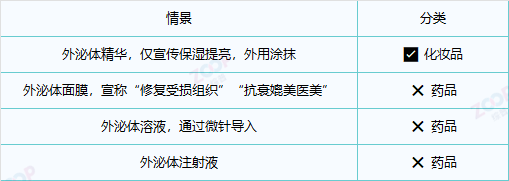
4. 加拿大的监管要求
1)上市前需获批(NOC、DIN)
2)临床研究阶段需获得“No Objection Letter (NOL)”
3)未获批产品存在感染传播风险、未经验证的疗效风险
化妆品类产品
1)企业需在首次销售后10天内备案
2)备案 ≠ 审批,也不代表产品一定合规
3)企业需自行确保符合《食品与药品法》及《化妆品法规》
5. 卫生部提醒与公众参与
1)未经授权的外泌体产品可能存在不实疗效宣传、潜在毒性、传染病风险
2)公众可通过加拿大卫生部平台投诉或报告不良事件
公众咨询期:
自通告发布起 75 天内,企业、从业者和消费者可提交意见或科学数据,供政策完善参考。
6. 总结
● 说“护肤美容”,还能作为化妆品备案
● 说“治疗修复”,那就是药品管理
对于企业而言,如何定位和宣传产品,将直接决定它的监管身份与合规风险。
对于消费者来说,买到的“外泌体精华”究竟是“护肤品”还是“药品”,未来可能会越来越清晰。
综普提供的服务
◆ 普通化妆品及天然健康产品、非处方药通报
◆ 产品配方及标签审核
◆ 产品安全证明所需测试以及安全评估服务
◆ 化妆品分类界定服务
◆ 加拿大化妆品法规符合性培训
◆ 其他客户定制服务